In più di a tecnulugia, a sintesi di glycosides hè sempre stata di interessu à a scienza, postu chì hè una reazione assai cumuna in a natura.Articuli recenti di Schmidt è Toshima è Tatsuta, è ancu parechje referenze citate quì, anu cummentatu una larga gamma di putenziali sintetici.
In a sintesi di glicosidi, un cumpunenti multi-zuccheru hè cumminatu cù un nucleophiles, cum'è l'alcooli, carbuidrati, o proteini, se una reazione selettiva cù unu di i gruppi idrossilici di un carbuidratu hè necessariu, tutte l'altri funzioni devenu esse prutetti in u corpu. primu passu.In principiu, i prucessi enzimatici o microbichi, per via di a so selettività, ponu rimpiazzà i passi cumplessi di prutezzione chimica è di deprotection à selettivamenti da i glucosides in regioni.In ogni casu, per via di a longa storia di alkyl glycosides, l'applicazione di l'enzimi in a sintesi di glycosides ùn hè micca stata largamente studiata è applicata.
A causa di a capacità di i sistemi enzimatici adattati è i costi di produzzione elevati, a sintesi enzimatica di poliglicosidi alchilici ùn hè micca pronta per esse aghjurnata à u livellu industriale, è i metudi chimichi sò preferiti.
In u 1870, MAcolley hà informatu a sintesi di "acetochlorhydrose" (1, figura 2) per a reazione di dextrose (glucose) cù acetyl chloride, chì eventualmente hà purtatu à a storia di e rotte di sintesi di glicoside.
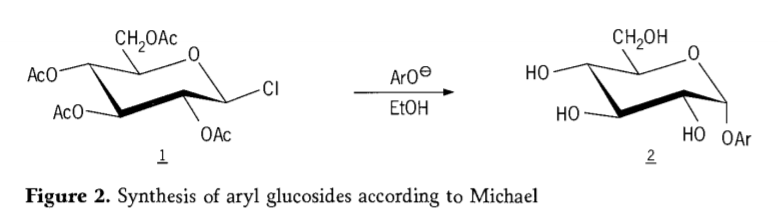
L'alogenuri di tetra-0-acetyl-glucopyranosyl (acetohaloglucoses) sò stati dopu truvati intermedi utili per a sintesi stereoselettiva di alchil glucosides puri.In u 1879, Arthur Michael hà riesciutu à preparà l'aryl glycosides cristallizabili definiti da l'intermedii è i fenolati di Colley.(Aro-, Figura 2).
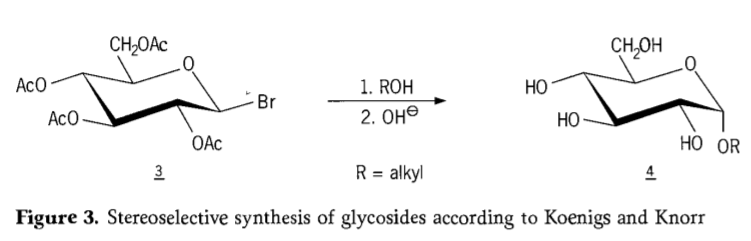
In u 1901, a sintesi di Michael à una larga gamma di carbuidrati è agliconi idrossilici, quandu W.Koenigs è E.Knorr introduciu u so prucessu di glycosidation stereoselective (Figura 3).A reazzione implica una sustituzzioni SN2 à u carbonu anomericu è prucede stereoselectively cù l'inversione di cunfigurazione, pruducia per esempiu l'α-glucoside 4 da u β-anomeru di l'intermediu aceobromoglucose 3. A sintesi di Koenigs-Knorr si faci in presenza di argentu o di l'argentu. i promotori di mercuriu.
In u 1893, Emil Fischer hà prupostu un approcciu fundamentale differente à a sintesi di l'alkyl glucosides.Stu prucessu hè oghji ben cunnisciutu com'è "glicosidazione di Fischer" è comprende una reazione catalizzata da l'acidu di glicosi cù l'alcooli.Qualchese cuntu storicu deve ancu include ancu u primu tentativu di A.Gautier in u 1874, per cunvertisce a destrosa cù etanolu anidru in presenza di l'acidu cloridicu.Grâce à une analyse élémentaire trompeuse, Gautier croyait avoir obtenu un "diglucose".Fischer a ensuite démontré que le « diglucose » de Gautier était en fait principalement de l'éthylglucoside (Figure 4).
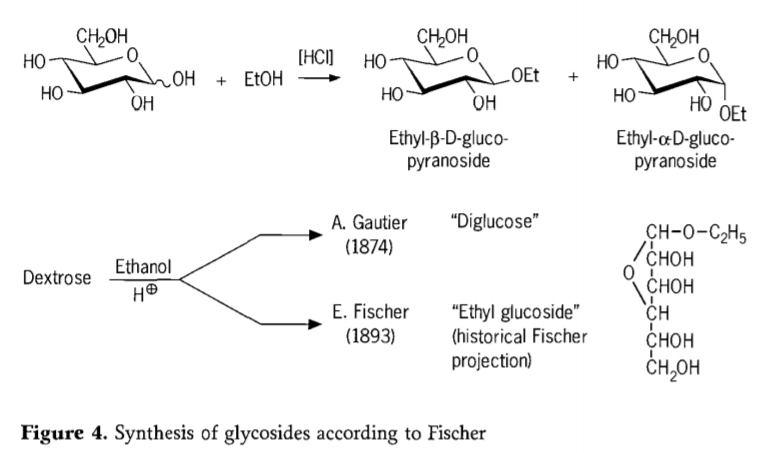
Fischer hà definitu a struttura di l'ethyl glucoside currettamente, cum'è pò esse vistu da a furanosidica furanosa storica pruposta.In fattu, i prudutti di glycosidation di Fischer sò cumplessi, soprattuttu mischi di equilibriu di α/β-anomers è isomeri pyranoside/furanoside chì includenu ancu oligomeri di glycoside ligati aleatoriamente.
In cunsiquenza, e spezie molekulari individuali ùn sò micca faciuli à isolà da i mischi di reazzione di Fischer, chì hè statu un prublema seriu in u passatu.Dopu qualchì migliuramentu di stu metudu di sintesi, Fischer hà aduttatu dopu a sintesi di Koenigs-Knorr per e so investigazioni.Aduprendu stu prucessu, E.Fischer è B.Helferich sò stati u primu t rapportu a sintesi di un alkyl glucoside à longa catena chì mostra proprietà surfactant in u 1911.
Finu à u 1893, Fischer avia rimarcatu currettamente e proprietà essenziali di i glicosidi alchilici, cum'è a so alta stabilità versu l'ossidazione è l'idrolisi, in particulare in i media fortemente alkalini.E duie caratteristiche sò preziose per i poliglicosidi alchilici in applicazioni di tensioattivi.
A ricerca ligata à a reazione di glicosidazione hè sempre in corso è parechje rotte interessanti à i glicosidi sò stati sviluppati in u passatu ricenti.Alcune di e prucedure per a sintesi di glicosidi sò riassunte in a Figura 5.
In generale, i prucessi di glicosidazione chimica ponu esse divisi in prucessi chì portanu à equilibri oligomeri cumplessi in u scambiu di glycosyl catalizatu da l'acidu.
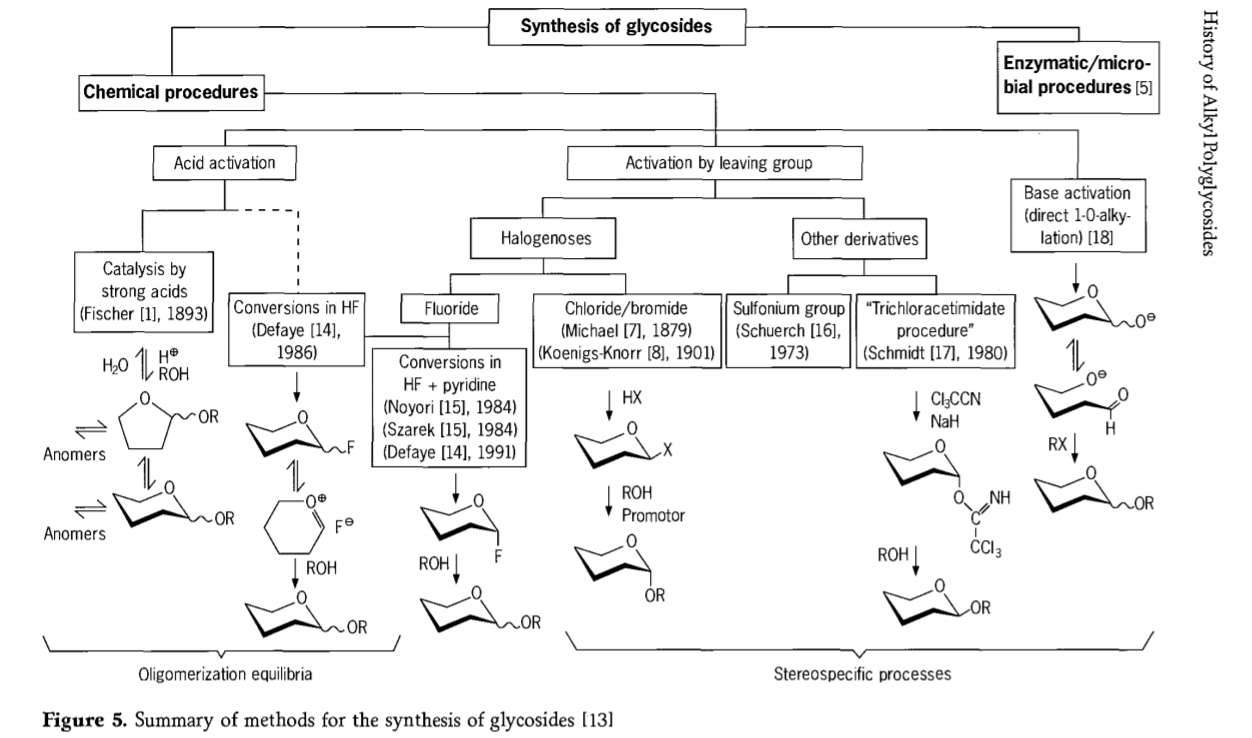
Reazioni nantu à i sustrati di carbuidrati attivati in modu adattatu (reazioni di Fischer glycosidic è reazioni di fluoruru di l'idrogenu (HF) cù molécule di carbuidrati senza prutezzione) è reazzioni di sostituzione cuntrullata, irreversibile, è principalmente stereotaxic cinetica cuntrullata.Un secondu tipu di prucedura pò guidà à a furmazione di spezie individuali in quantu à mischii cumplessi di reazzioni, soprattuttu quandu cumminati cù tecniche di gruppu di cunservazione.I carbuidrati ponu lascià gruppi nantu à u carbonu ectopicu, cum'è l'atomi d'alogenu, sulfonyls, o gruppi trichloroacetimidate, o esse attivati da basi prima di cunversione à esteri triflati.
In u casu particulari di glicosidazioni in fluoruri di l'idrogenu o in mischi di fluoruri di l'idrogenu è piridine (piridiniu poly [fluoruri di l'idrogenu]), i fluoruri di glicosil sò furmati in situ è sò cunvertiti bè in glicosidi, per esempiu cù l'alcooli.U fluoruru di l'idrogenu hè statu dimustratu per esse un mediu di reazione forte attivante è non degradante;equilibriu auto condensation (oligomerization) hè osservatu simile à u prucessu di Fischer, puru siddu lu meccanismi di reazzione hè prubabilmente differente.
I glicosidi alchilici chimicamente puri sò adattati solu per applicazioni assai speciali.Per esempiu, glicosidi alchilici sò stati aduprati cù successu in a ricerca biochimica per a cristallizazione di proteine di membrana, cum'è a cristallizazione tridimensionale di porina è bacteriorhodopsin in presenza di octyl β-D-glucopyranoside (ulteriori esperimenti basati nantu à stu travagliu portanu à u Nobel). Premiu di chimica per Deisenhofer, Huber è Michel in u 1988).
In u corsu di u sviluppu di l'alkyl polyglycosides, i metudi stereoselettivi sò stati aduprati à una scala di laboratoriu per sintetizà una varietà di sustanzi mudelli è studià e so proprietà fisicochimiche, per via di a so cumplessità, l'instabilità di l'intermedii è a quantità è a natura critica di u prucessu. wasters, sintesi di u tipu Koenigs-Knorr è altri tecnichi di gruppu protettivu creanu prublemi tecnichi è ecunomichi significativi.I prucessi di tipu Fischer sò comparativamente menu cumplicati è più faciuli di fà in una scala cummerciale è per quessa, sò u metudu preferitu per a produzzione di poliglicosidi alchili à grande scala.
Tempu di pubblicazione: 12-settembre-2020





